Reaksi keseimbangan basa dengan rumus umum A dapat dituliskan. Adanya ion senama menurunkan ionisasi asam lemah atau basa lemah.
 Penurunan Rumus Hidrolisis Garam Asam
Penurunan Rumus Hidrolisis Garam Asam
M atau OH K b.
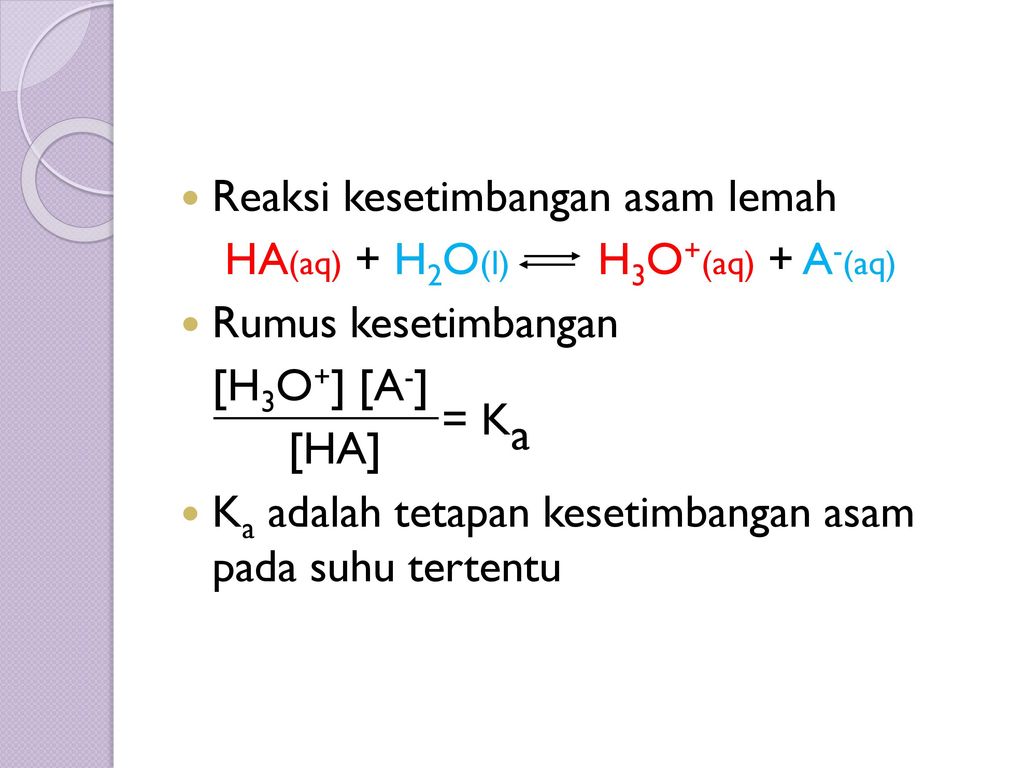
Rumus tetapan kesetimbangan asam basa. Rumus tetapan hidrolisis garam yang berasal dari asam kuat dan basa kuat. H 3 O 6 x 10 -3 M. NH4Cl Garam Pada reaksi tersebut molekul HCl bertindak sebagai donor proton asam dan molekul NH3 bertindak sebagai akseptor proton basa.
Senyawa paling banyak diproduksi Sulfuric acid H2SO4 Asam sulfat Hydrochloric acid HCl Asam Klorida Nitric acid HNO3 Asam Nitrat Sodium Hydroxide NaOH Basa Natrium hidroksida Calcium hydroxide CaOH2 Basa Kalsium hidroksida Ammonia NH3 bakal Basa. CH3COONa s Naaq CH 3COO-aq CH3COOH aq Haq CH 3COO. K b L OH LOH Dengan keterangan L OH maka LOH M maka.
Efekionsenama adalah pergeseran kesetimbangan yang disebabkan oleh penambahan senyawa yang memiliki ion yang sama zat yang dilarutkan. Tetapan kesetimbangan Ionisasi Basa Lemah K b dapat dinyatakan dengan menggunakan persamaan rumus berikut. Larutan garam dari asam lemah dan basa.
Menurut Brownsted- Lowry reaksi asam basa yang melibatkan transfer proton membentuk keadaan kesetimbangan. Tetapan kesetimbangan Ionisasi Basa Lemah K b dapat dinyatakan dengan menggunakan persamaan rumus berikut. K b OH 2 M OH 2 K b.
M Dengan menggunakan cara yang sama pda asam lemah maka diperoleh derajat ionisasi basa lemah. Ka tetapan ionisasi asam lemah a jumlah mol asam lemah g jumlah mol basa konjugasi Rumus pH Larutan Buffer Basa. M Dengan menggunakan cara yang sama pda asam lemah maka diperoleh derajat ionisasi basa.
Rumus tetapan hidrolisis Kh adalah sebagai berikut. Kb tetapan ionisasi basa lemah b konsentrasi basa lemah. Perhatikan campuran CH3COONa elektrolit kuat dan CH3COOH asam lemah.
X 18 x 10 -5 x 2 12 6 x 10 -3. K a 18 x 10 -5 x x 2 x x x 2 18 x 10 -5 x 2 2. K b L OH LOH Dengan keterangan L OH maka LOH M maka.
K b OH 2 M OH 2 K b. HCl g NH3 g NH4Cl s HCl Asam. Rumus tetapan hidrolisis garam yang berasal dari asam kuat dan basa.
M atau OH K b. Untuk mencari tetapan ionisasi dari asam laktat tersebutkita bisa menggunakan rumus yang telah kita buat sebelumnya yaitu. Untuk basa tetapan keseimbangan diidentifikasi sebagai tetapan ionisasi basa Kb.
Konsentrasi ion H dari asam laktat bisa kita dapatkan dari PH nya dengan cara. A aq H 2 O l HA aq OH aq Oleh karena itu rumus tetapan keseimbangan ionisasinya adalah Kb HA OH A dan secara sama p Kb log Kb. RUMUS H ASAM LEMAH RUMUS OH- BASA LEMAH.
Penambahan ion sejenis ke dalam larutan garam yang terhidrolisis akan membentuk larutan penyangga. Campuran tersebut juga dapat mempertahankan harga pH walaupun air sungai yang mengalir ke laut bersifat asam atau basa. OH- Kb x bvalxg atau pOH p Kb - log bg pH 14 - pOH Ket.
Tetapan kesetimbangan untuk garam-garam yang terhidrolisis dapat ditentukan melalui persamaan K w K a K b. Untuk menghitung pH asam lemah dan basa lemah diperlukan tetapan kesetimbangan Ka atau Kb terutama sekali. Sehingga rumusan tetapan keseimbangan ionisasinya adalah K a H 3 O A- HA Karena niai tetapan melibatkan numerik dengan pangkat eksponen sangat kecil hingga sangat besar maka ukuran kuantitatif kekuatan asam lebih sering dinyatakan dalam pK a p potent dengan pK a - log K a.
Larutan garam dari asam kuat dan basa kuat seperti NaCl KNO 3 Na 2 SO 4 dan lain lain bersifat netral. Menurut Teori Asam Basa Arrhenius larutan penyangga adalah campuran asam lemah dan garamnya atau basa lemah dan garamnya. Karena perbandingan H dan OH sama maka larutan bersifat netral sehingga kita tidak memerlukan Kh untuk menghitung pH larutan tersebut karena sudah dipastikan pH 7.
Selanjutnya kita dapat menentukan nilai x yang sama dengan nilai H 3 O. KESETIMBANGAN ASAM BASA SMAN PINTAR KUANSING Oleh. Persamaan konstanta kesetimbangan asam lemah sekarang dapat dituliskan sebagai berikut.
H Ka x avalxg atau pH p Ka - log ag Ket. Karena tidak membentuk kesetimbangan seperti anion dan kation dari asam dan basa lemah. Kesetimbangan Asam Basa 1.
Di bawah ini adalah rumusnya. Ka Konsentrasi ion H 2 Konsentrasi Asam Lemah M Ket. Kesetimbangan Ion dalam Larutan Asam Basa Air yang ada di alam seperti air laut merupakan campuran berbagai macam larutan garam yang dapat memengaruhi pH.
CH3COO-aq Haq CH3COOHaq Rumus pH Larutan Buffer Asam.
 Kekuatan Asam Basa Dan Ph Larutan Kimia Kelas Xi
Kekuatan Asam Basa Dan Ph Larutan Kimia Kelas Xi
 Teori Asam Basa Arhenius Ppt Download
Teori Asam Basa Arhenius Ppt Download
 Larutan Asam Basa Kekuatan Derajat Keasaman Contoh Soal
Larutan Asam Basa Kekuatan Derajat Keasaman Contoh Soal
 Konstanta Kesetimbangan Rumus Soal Dan Jawaban Pinterpandai
Konstanta Kesetimbangan Rumus Soal Dan Jawaban Pinterpandai
 Satuan Rumus Tetapan Kesetimbangan Air Ardra Biz
Satuan Rumus Tetapan Kesetimbangan Air Ardra Biz
 Kesetimbangan Asam Dan Basa Ppt Download
Kesetimbangan Asam Dan Basa Ppt Download
 Tetapan Kesetimbangan Asam Basa Ilmu Kimia Artikel Dan Materi Kimia
Tetapan Kesetimbangan Asam Basa Ilmu Kimia Artikel Dan Materi Kimia
 Tuliskan Bentuk Rumus Tetapan Kesetimbangan Kc Pada Reaksi Berikut A C S Co2 G 2co G Mas Dayat
Tuliskan Bentuk Rumus Tetapan Kesetimbangan Kc Pada Reaksi Berikut A C S Co2 G 2co G Mas Dayat
Ppt 2 Flip Ebook Pages 1 17 Anyflip Anyflip
 Tetapan Ionisasi Asam Basa Prodi Bioteknologi Fakultas Ilmu Ppt Download
Tetapan Ionisasi Asam Basa Prodi Bioteknologi Fakultas Ilmu Ppt Download
 Kesetimbangan Asam Basa Ppt Download
Kesetimbangan Asam Basa Ppt Download
 Tuliskan Rumus Tetapan Kesetimbangan Konsentrasi Untuk Reaksi Berikut Tolong Dibantuin Ya Brainly Co Id
Tuliskan Rumus Tetapan Kesetimbangan Konsentrasi Untuk Reaksi Berikut Tolong Dibantuin Ya Brainly Co Id
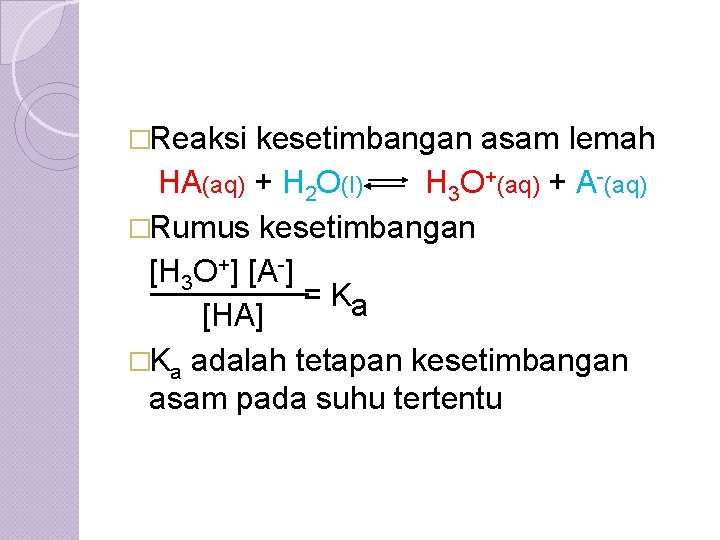 Kesetimbangan Asam Basa Referensi Prinsipprinsip Kimia Modern Penulis
Kesetimbangan Asam Basa Referensi Prinsipprinsip Kimia Modern Penulis

 Kesetimbangan Asam Basa Ppt Download
Kesetimbangan Asam Basa Ppt Download
 Tetapan Kesetimbangan Basa Hs Kbhs Diperoleh Reaksi Brainly Co Id
Tetapan Kesetimbangan Basa Hs Kbhs Diperoleh Reaksi Brainly Co Id
 Kesetimbangan Asam Basa Ppt Download
Kesetimbangan Asam Basa Ppt Download

 Ph Larutan Dan Reaksi Ionisasi Air
Ph Larutan Dan Reaksi Ionisasi Air