Satuan laju reaksi adalah Ms Molar per detik. LAJU REAKSI -PETA KONSEP- Laju Reaksi adalah perubahan konsentrasi reaktan atau produk per satuan waktu.
 Persamaan Laju Reaksi Penjelasan Rumus Contoh Soal Dan Jawaban
Persamaan Laju Reaksi Penjelasan Rumus Contoh Soal Dan Jawaban
Kita dapat menentukan reaktan mana yang lebih mempengaruhi laju reaksi ingat tentang orde reaksi.

Satuan tetapan laju reaksi orde 3. Persamaan laju reaksi reaksi tersebut adalah v kAB ½ Jika konsentrasi dinyatakan dalam mol L 1 dan satuan dalam menit tentukan satuan untuk tetapan laju reaksinya. A B k C D Memiliki konstanta laju reaksi k dalam satuan mol-1literdetik-1 sehingga reaksi tersebut adalah 1 Orde satu terhadap A dan orde satu terhadap B 2 Orde dua terhadap A dan orde nol terhadap B 3 Orde nol terhadap A dan orde dua terhadap B 4 Orde satu terhadap C dan orde satu terhadap D 2. Untuk reaksi aA bB cC dD persamaan laju.
K tetapan laju reaksi m ordetingkat reaksi terhadap A n ordetingkat reaksi terhadap B A konsentrasi awal A mol Liter. Jelaskan pengertian tentang laju reaksi 2. Tentukan orde laju reaksi 4.
Laju Reaksi 4 F. Jadi ordenya secara keseluruhan adalah 1 2 3. Alat dan Bahan Pada percobaan ini digunakan alat-alat yakni pipet volumetrik 10 mL labu erlenmeyer 250 mL bertutup buret 50 mL botol semprot hot plate termometer stopwatch konduktometer.
2 y 2 y 1 reaksi orde 1 terhadap Br 2Jadi rumus kecepatan reaksinya. Laju reaksi semakin besar dengan penggunaan katalis SEBAB Katalis dapat. Dengan menggunakan rumus umum tertentu ini dapat dengan muda.
Tetapan k yang muncul disebut juga sebagai tetapan laju atau koefisien laju. Karena nilai k belum dketahui maka bisa menggunakan Fitur variance untuk nilai k dari nilai t0 sampai tt 6. V kNO 2 Br 2 12 k01 2 01 k 12 x 10 3 mol-2 1 2 det-1 Faktor faktor yang mempengaruhu laju reaksi.
3 LAJU REAKSI Setelah mempelajari bab ini kamu diharapkan mampu. Orde reaksi adalah Bilangan pangkat yang menyatakan hubungan konsentrasi zat pereaksi dengan laju reaksi. Salah satu cara memperkirakan orde reaksi dengan memperhatikan satuan nilai tetapan laju reaksi.
Perubahan konsentrasi reaktan itu tidak mempengaruhi laju reaksi. Orde reaksi di sini 1 dan 2 berbeda dengan koefisien stoikiometrinya 2 dan 1. Dihitung semua variable dalam persamaan 3.
Laju berkurangnya reaktan atau bertambahnya produk yang dinyatakan dalam molardetik. Misalnya jika konsentrasi reaktan ditingkatkan 3 kali semula maka laju reaksi juga akan meningkat 3 kali dari semula. Dari percobaan tersebut akan diperoleh data yang nantinya dapat digunakan untuk penentuan laju reaksi.
Jelaskan faktor-faktor yang mempengaruhi laju reaksi berdasarkan analisis percobaan Kim. Tentukan persamaan laju reaksi 3. Satuan laju reaksi umumnya dinyatakan dengan molliterdetik.
Tentukan tetapan laju reaksi 5. Ia hanya bisa ditentukan lewat percobaan. Orde reaksi nol.
Laju reaksi tidak bisa ditentukan secara teoritis melainkan melalui percobaan. Jelaskan fakor-faktor yang mempengaruhi laju reaksi berdasarkan teori tumbukan 6. Dalam contoh ini reaktan HgCl 2 adalah 1 dan ion oksalat adalah 2.
Orde reaksi terhadap A 1 dan orde reaksi terhadap B 12 orde reaksi keseluruhan n 1 ½ 1½ atau 32. Reaksi dikatakan berorde nol terhadap salah satu reaktan jika perubahan konsentrasi reaktan tersebut tidak mempengaruhi laju reaksi. Contohnya reaksi kimia antara raksa II klorida dengan ion oksalat.
Orde Reaksi 0 1 2 Nol Satu Dua Negatif Persamaan Laju Reaksi Pengertian Grafik Rumus Contoh Soal Pembahasan Kimia - Pada umumnya hubungan antara laju reaksi dengan konsentrasi zat-zat pereaksi hanya diturunkan dari data eksperimen. Jelaskan faktor-faktor yang mempengaruhi laju reaksi berdasarkan analisis percobaan. Artinya asalkan terdapat dalam jumlah tertentu.
Konstanta laju reaksi k. Di plot sesuai persamaan membentuk garis yax 4. V kNO 2 Br 2 reaksi orde 3 b.
Satuan tetapan jenis reaksi k tergantung pada tingkat reaksi. Orde reaksi terhadap A dan B masing-masing adalah. Setiap kenaikan suhu 20 0 C laju reaksi menjadi 3 kali lebih cepat dari semula.
Persamaan laju reaksinya adalah r kHgCl 2 1 C 2 O 4 2 2. Laju reaksi didefinisikan sebagai perubahan konsentrasi reaktan atau produk per satuan waktu. Untuk menentukan nilai k cukup kita ambil salah satu data percobaan saja misalnya data 1 maka.
Satuan tetapan atau koefisien laju bergantung pada orde reaksi. Reaksi Orde ke-n 1. Besarnya laju reaksi hanya dipengaruhi oleh besarnya konstanta laju reaksi k.
Jelaskan fakor-faktor yang mempengaruhi laju reaksi berdasarkan teori tumbukan 6. Tentukan orde laju reaksi 4. Persamaan diselesaikan dengan menebak nilai n 2.
Tentukan persamaan laju reaksi 3. Tentukan tetapan laju reaksi 5. Reaksi orde tiga mempunyai satuan tetapan laju reaksi.
Pada reaksi kimia dengan orde satu besarnya laju reaksi berbanding lurus dengan besarnya konsentrasi reaktan.
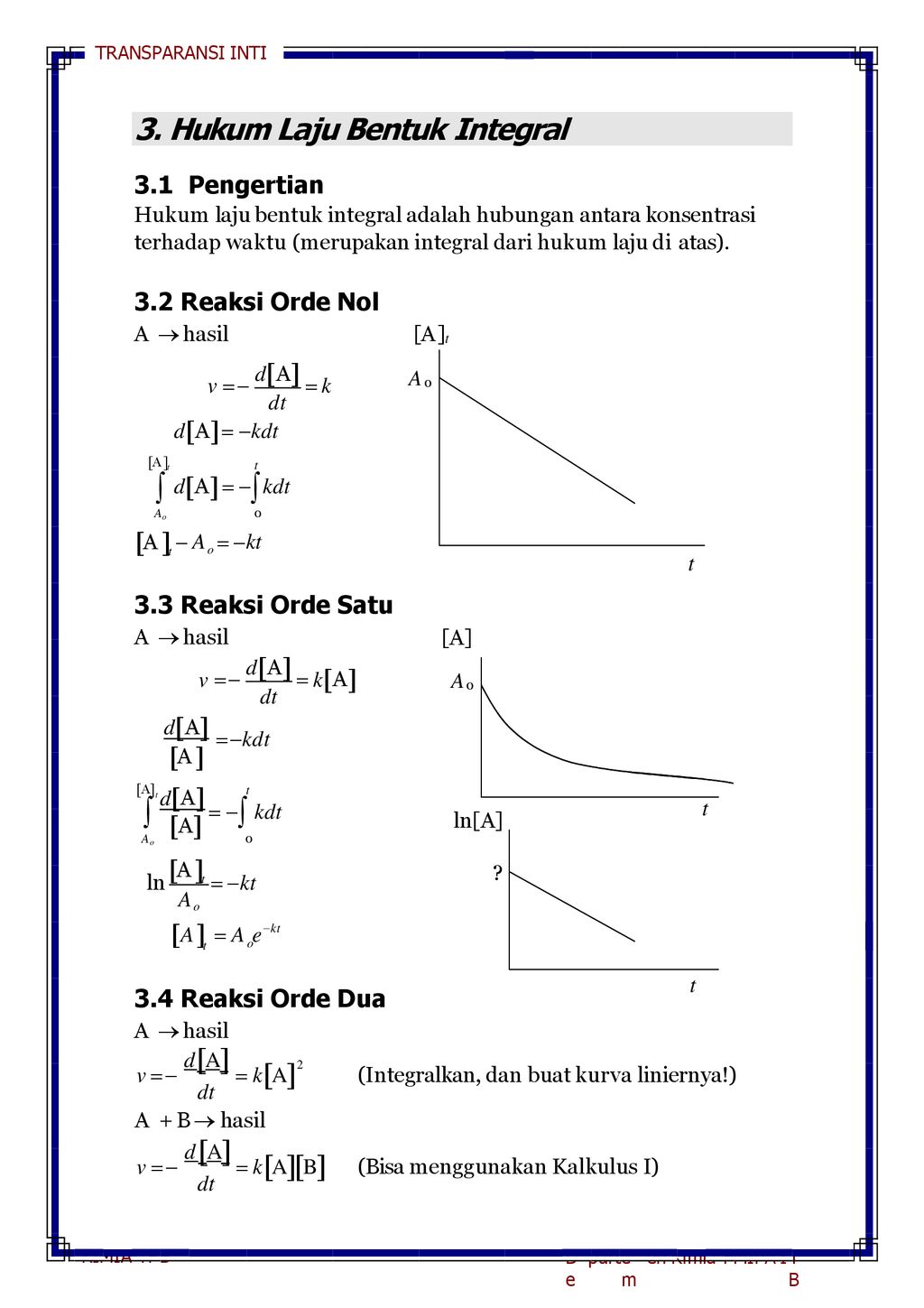 D A V D B D C 1 Laju Reaksi 2 Hukum Laju Dan Orde Reaksi Ppt Download
D A V D B D C 1 Laju Reaksi 2 Hukum Laju Dan Orde Reaksi Ppt Download
 Memahami Grafik Tentang Laju Reaksi Dan Variasi Soal Urip Dot Info
Memahami Grafik Tentang Laju Reaksi Dan Variasi Soal Urip Dot Info
 Kinetika Reaksi Tri Yulianti Sf Apt Ppt Download
Kinetika Reaksi Tri Yulianti Sf Apt Ppt Download
 Reaksi Orde Tiga Mempunyai Satuan Tetapan Laju Reaksi Brainly Co Id
Reaksi Orde Tiga Mempunyai Satuan Tetapan Laju Reaksi Brainly Co Id
 Rumus Laju Reaksi Orde Nol Edukasi Lif Co Id
Rumus Laju Reaksi Orde Nol Edukasi Lif Co Id
 Memahami Grafik Tentang Laju Reaksi Dan Variasi Soal Urip Dot Info
Memahami Grafik Tentang Laju Reaksi Dan Variasi Soal Urip Dot Info
 Rumus Laju Reaksi Orde 1 Edukasi Lif Co Id
Rumus Laju Reaksi Orde 1 Edukasi Lif Co Id
 Kinetika Kimia Bab X Kinetika Kimia 1 Laju
Kinetika Kimia Bab X Kinetika Kimia 1 Laju
 Standar Kompetensi 3 Memahami Kinetika Reaksi Kesetimbangan Kimia
Standar Kompetensi 3 Memahami Kinetika Reaksi Kesetimbangan Kimia

 Memahami Grafik Tentang Laju Reaksi Dan Variasi Soal Urip Dot Info
Memahami Grafik Tentang Laju Reaksi Dan Variasi Soal Urip Dot Info
 Menentukan Satuan Tetapan Laju Reaksi Orde Pertama Ksm 2014 Kabupaten Kota Youtube
Menentukan Satuan Tetapan Laju Reaksi Orde Pertama Ksm 2014 Kabupaten Kota Youtube
 Pengantar Kinetika Kimia Ii Orde Reaksi Waktu Paruh Ppt Download
Pengantar Kinetika Kimia Ii Orde Reaksi Waktu Paruh Ppt Download
 Menentukan Nilai Dan Satuan Konstanta Laju Reaksi Laju Reaksi Part 21 Youtube
Menentukan Nilai Dan Satuan Konstanta Laju Reaksi Laju Reaksi Part 21 Youtube
 Persamaan Laju Reaksi Dan Grafik Orde Konsep Mudah Youtube
Persamaan Laju Reaksi Dan Grafik Orde Konsep Mudah Youtube



