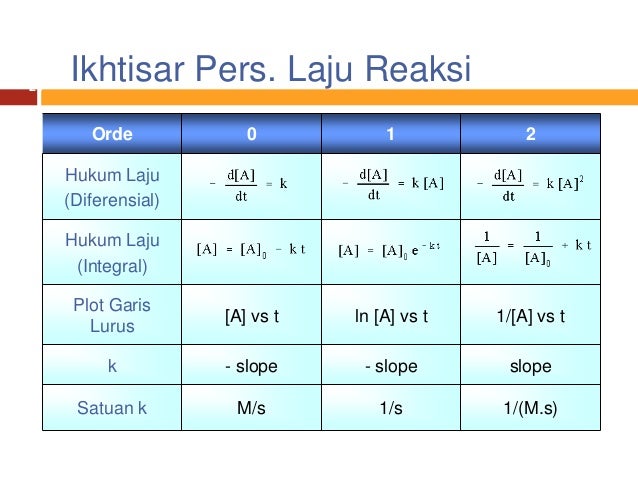
Hukum laju reaksi merupakan hubungan antara laju reaksi dengan konsentrasi awal zat-zat pereaksi. D k 37 10 3 L 2 mol 2.
 Menentukan Satuan Tetapan Laju Reaksi Orde Pertama Ksm 2014 Kabupaten Kota Youtube
Menentukan Satuan Tetapan Laju Reaksi Orde Pertama Ksm 2014 Kabupaten Kota Youtube
Tentukan masing-masing orde reaksi dari suatu persamaan reaksi yang diketahui nilai tetapan laju reaksi k seperti berikut ini.

Satuan tetapan laju reaksi k untuk reaksi orde 2 adalah. A k 32 10 4 s 1. Pada reaksi kimia dengan orde nol laju reaksi akan tetap walaupun telah dilakukan perlakuan terhadap konsentrasi reaktannya. 2NO2 g - 2NO g O2 g pada suhu 300 C adalah 054 M-1s-1.
Rabu 17 Oktober 2018. Faktor k yang terdapat pada persamaan tersebut disebut tetapan reaksi. Tetapan laju reaksi untuk reaksi orde 2.
Hukum laju reaksi dapat digunakan untuk menghitung laju suatu reaksi melalui data konstanta laju reaksi dan konsentrasi reaktan. K merupakan tetapan laju reaksi yang nilainya tetap pada suhu tetap. Reaksi orde kedua adalah reaksi yang lajunya bergantung pada konsentrasi salah satu reaktan dipangkatkan dua atau pada konsentrasi dua reaktan berbeda yang masing-masing dipangkatkan satu.
Mn orde reaksi bilangan pangkat yang menyatakan besarnya pengaruh konsentrasi A B terhadap laju reaksi. Persamaan laju reaksi untuk reaksi orde dua adalah. Untuk menentukan nilai k cukup kita ambil salah satu data percobaan saja misalnya data 1 maka.
C k 43 10 5 L mol 1 s 1. M detik -1 M-1 detik M-2 detik -2 M-1 detik-1. Nilai k berbanding lurus dengan laju reaksi semakin besar nilainya maka semakin cepat reaksi tersebut berjalan.
Setiap reaksi mempunyai harga k tertentu pada suhu tertentu harganya akan berubah bila suhu diubah. Karena reaksi tersebut berorde 2 maka persamaan laju reaksinya adalah. Besarnya orde reaksi tergantung dari besarnya laju reaksi apabila diberi perlakuan terhadap konsentrasi reaktannya.
Kita akan mempelajari laju reaksi dengan orde reaksi satu dua dan nol. Satuan tetapan atau koefisien laju bergantung pada orde reaksi. Berapa tetapan laju reaksi agar konsentrasi NO2 berkurang dari 062 M menjadi 028 M.
Maka hukum laju dinyatakan dengan rumus berikut. K tetapan laju reaksi. Hukum laju reaksi juga dapat digunakan untuk menentukan konsentrasi reaktan setiap saat selama reaksi kimia berlangsung.
R k A2 Apabila suatu reaksi berorde dua terhadap suatu pereaksi berarti laju reaksi itu berubah secara kuadrat terhadap perubahan konsentrasinya. Apabila konsentrasi zat A dinaikkan misalnya 2 kali maka laju reaksi akan menjadi 22 atau 4 kali lebih besar. V k Am Bn.
Konstanta laju reaksi didefinisikan sebagai. V k NO₂² V 054 062² 0208. Harga k ini tetap untuk suatu reaksi dan hanya dipengaruhi oleh suhu dan katalis.
Apakah ada yang tahu hukum laju reaksi dan orde reaksi. 2 y 2 y 1 reaksi orde 1 terhadap Br 2Jadi rumus kecepatan reaksinya. Dalam kimia dijelaskan bahwasanya laju reaksi adalah adalah besarnya perubahan jumlah pereaksi dan hasil reaksi per satuan waktu.
Sekarang kalian perhatikan dan pahami penjelasan mengenai hukum laju dan orde reaksi. Jenis yang paling sederhana hanya melibatkan satu molekul reaktan. Laju reaksi adalah perubahan konsentrasi pereaksi ataupun produk dalam satu satuan waktu.
Perubahan ini dapat dikatakan perubahan konsentrasi molar molaritas sehingga laju reaksi dapat dikatakan perubahan konsentrasi akhir hasil reaksi terhadap konsentrasi awal pereaksi per satuan waktu. V laju reaksi mol L -1 s -1. Untuk reaksi orde I v kA satuan v adalah mol dm-3 s-1 dan A adalah mol dm-3 sehingga satuan dari k untuk reaksi orde satu adalah s-1 Mulyani 2004160.
Artinya jika reaksi dilakukan pada suhu yang sama maka nilai tetapan laju. V kNO 2 Br 2 reaksi orde 3 b. V kNO 2 Br 2 12 k01 2 01 k 12 x 10 3 mol-2 1 2 det-1 Faktor faktor yang mempengaruhu laju reaksi.
Secara umum persamaan laju reaksi dapat dituliskan sebagai berikut. Satuan tetapan jenis reaksi k tergantung pada tingkat reaksi. K 12 Ms.
Pada umumnya harga orde reaksi merupakan bilangan bulat sederhana yaitu 1 2 atau 3 tetapi kadang-kadang juga terdapat pereaksi yang mempunyai orde reaksi 0 ½ atau bahkan negatif. Satuan tetapan jenis reaksi untuk reaksi tingkat 2 adalah. Laju reaksi dinyatakan sebagai laju berkurangnya konsetrasi suatu pereaksi atau laju bertambahnya suatu produk.
B k 65 10 2 mol L 1 s 1. Tetapan jenis reaksi adalah suatu konstanta atau tetapan yang harganya bergantung pada jenis pereaksi suhu dan katalis.
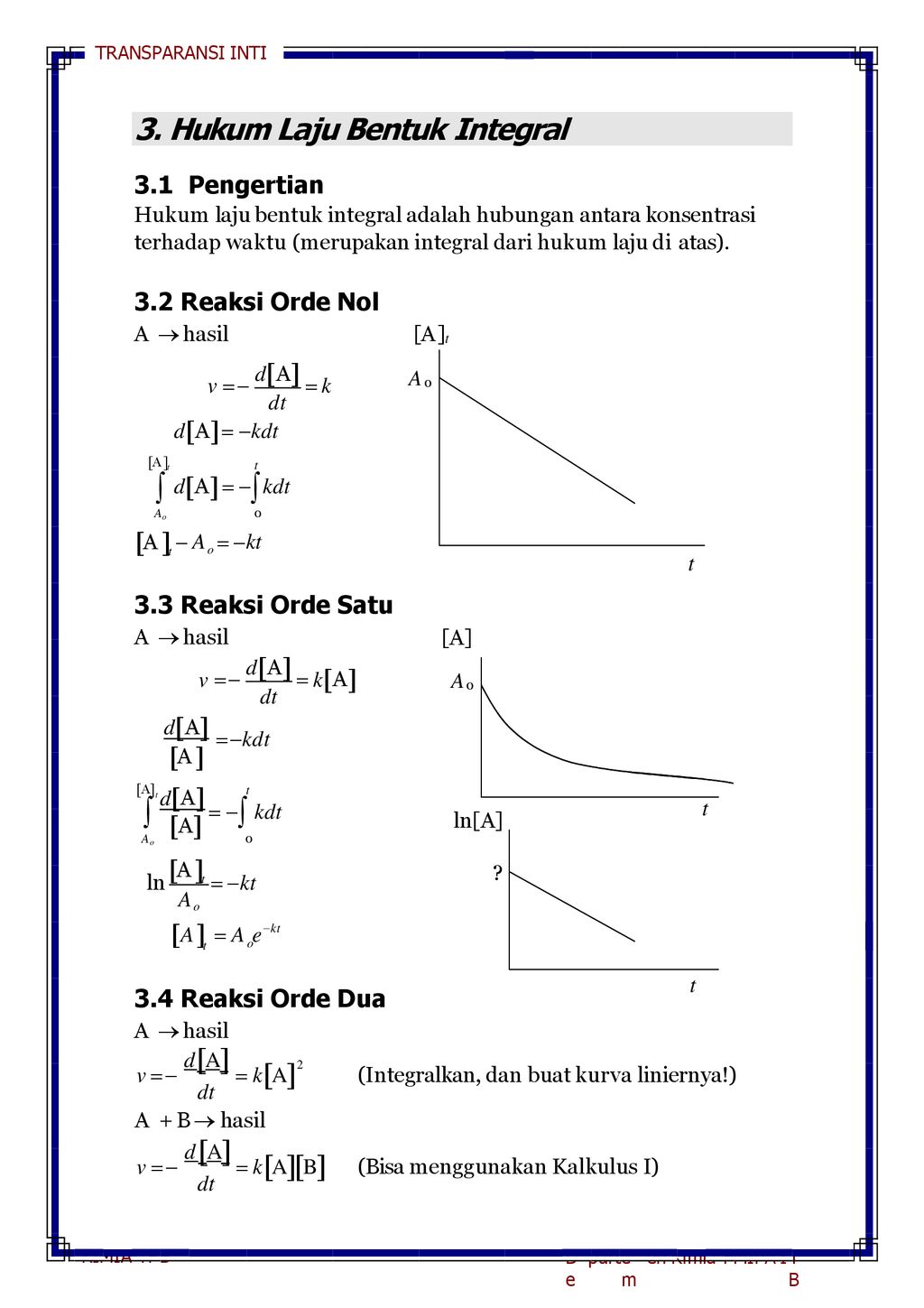 D A V D B D C 1 Laju Reaksi 2 Hukum Laju Dan Orde Reaksi Ppt Download
D A V D B D C 1 Laju Reaksi 2 Hukum Laju Dan Orde Reaksi Ppt Download
 Persamaan Laju Reaksi Penjelasan Rumus Contoh Soal Dan Jawaban
Persamaan Laju Reaksi Penjelasan Rumus Contoh Soal Dan Jawaban
 Tentukanlah A Persamaan Laju Reaksi B Harga Tetapan Laju Reaksi K Brainly Co Id
Tentukanlah A Persamaan Laju Reaksi B Harga Tetapan Laju Reaksi K Brainly Co Id
 Laju Reaksi Soal Orde Reaksi Persamaan Laju Reaksi Dan Harga K Kimia Sma Youtube
Laju Reaksi Soal Orde Reaksi Persamaan Laju Reaksi Dan Harga K Kimia Sma Youtube
 Tentukan Satuan Dari Tetapan Laju Reaksi Pada A Reaksi Orde 0 B Reaksi Orde 2 C Reaksi Orde 1 Brainly Co Id
Tentukan Satuan Dari Tetapan Laju Reaksi Pada A Reaksi Orde 0 B Reaksi Orde 2 C Reaksi Orde 1 Brainly Co Id
 Laju Reaksi Media Pembelajaran Kimia Xi Ipa
Laju Reaksi Media Pembelajaran Kimia Xi Ipa
 Satuan Tetapan Laju Reaksi Untuk Orde Satu Adalah Brainly Co Id
Satuan Tetapan Laju Reaksi Untuk Orde Satu Adalah Brainly Co Id
 Menentukan Nilai Dan Satuan Konstanta Laju Reaksi Laju Reaksi Part 21 Youtube
Menentukan Nilai Dan Satuan Konstanta Laju Reaksi Laju Reaksi Part 21 Youtube
 Kinetika Reaksi Tri Yulianti Sf Apt Ppt Download
Kinetika Reaksi Tri Yulianti Sf Apt Ppt Download
 Rumus Laju Reaksi Orde Nol Edukasi Lif Co Id
Rumus Laju Reaksi Orde Nol Edukasi Lif Co Id
 Diketahui Reaksi A 2 B C Dari Percobaan Diperoleh Data Sebagai Berikut Orde Reaksi Terhadap A Brainly Co Id
Diketahui Reaksi A 2 B C Dari Percobaan Diperoleh Data Sebagai Berikut Orde Reaksi Terhadap A Brainly Co Id
 Jika Tetapan Laju Reaksinya K Maka Persamaan Laju Reaksi V Dari P Dan Q Adalah Mohon Dijawab Brainly Co Id
Jika Tetapan Laju Reaksinya K Maka Persamaan Laju Reaksi V Dari P Dan Q Adalah Mohon Dijawab Brainly Co Id
 Reaksi Orde Tiga Mempunyai Satuan Tetapan Laju Reaksi Brainly Co Id
Reaksi Orde Tiga Mempunyai Satuan Tetapan Laju Reaksi Brainly Co Id

 Rumus Laju Reaksi Orde 1 Edukasi Lif Co Id
Rumus Laju Reaksi Orde 1 Edukasi Lif Co Id