Kb Konsentrasi ion OH- 2 Konsentrasi Basa Lemah M Ket. Untuk mencari tetapan ionisasi dari senyawa hidroksilamin tersebut kita bisa menggunakan rumus yang telah kita buat sebelumnya yaitu.
 Tetapan Kesetimbangan Basa Hs Kbhs Diperoleh Reaksi Brainly Co Id
Tetapan Kesetimbangan Basa Hs Kbhs Diperoleh Reaksi Brainly Co Id
Rumus tetapan hidrolisis Kh adalah sebagai berikut.

Rumus tetapan basa. α Derajat disosiasi basa. Garam dari Asam Kuat dan Basa Lemah. A aq H 2 O l HA aq OH aq Oleh karena itu rumus tetapan keseimbangan ionisasinya adalah Kb HA OH A dan secara sama p Kb log Kb.
A Konsentrasi ion H Konsentrasi asam lemah x 100 Karena pH nya tidak diketahui maka konsentrasi ion H nya harus kita cari dengan menggunakan rumus. 5 - log 6 Pembahasan. Reaksi keseimbangan basa dengan rumus umum A dapat dituliskan.
02 210-6 10-3. PH 14 - pOH 1125 14 - pOH. 4 - log 6 E.
Beberapa basa lemah dan nilai tetapan kesetimbangan basanya. Nilai Kb beberapa senyawa basa amonia amina dan enamina pada suhu 25 C. Garam dari Asam Lemah dan Basa Kuat.
H Ka x avalxg atau pH p Ka - log ag Ket. Nama Rumus Kimia Struktur Lewis Nilai Kb Dietilamina CH 3 CH 2 2 NH Dimetilamina CH 3 2 NH Metilamina CH 3 NH 2 Amonia NH 3 Piridin C 5 H 5 N Anilin C 6 H 5 NH 2 86 x 10-4 59 x 10-4 44 x 10-4 176. Untuk basa tetapan keseimbangan diidentifikasi sebagai tetapan ionisasi basa Kb.
C konsentrasi basa. Jika Ka Kb maka pH 7 dalam rumus di bawah adalah label ASAM. Pengertian Rumus Derajat Ionisasi Asam Basa Lemah Contoh Soal Perhitungan 9.
Ka tetapan ionisasi asam lemah a jumlah mol asam lemah g jumlah mol basa konjugasi Rumus pH Larutan Buffer Basa. Menurut Brownsted- Lowry reaksi asam basa yang melibatkan transfer proton membentuk keadaan kesetimbangan. Rumus tetapan hidrolisis garam yang berasal dari asam kuat dan basa.
PH hidrolisis ini tidak bergantung terhadap konsentrasi asam atau basa karena dalam spesi lemah asam lemah dan basa lemah nilai pH-nya ditentukan oleh tinggi atau rendahnya tetapan asambasa Ka atau Kb Jika Ka Kb maka pH 7. Al 2 SO 4 3 AgNO 3 CuSO 4 NH 4 Cl AlCl 3. Asam lemah akan mengalami ionisasi sebagian.
H Ka. RUMUS H ASAM LEMAH RUMUS OH- BASA LEMAH. NH4Cl Garam Pada reaksi tersebut molekul HCl bertindak sebagai donor proton asam dan molekul NH3 bertindak sebagai akseptor proton basa.
Untuk dapat menentukan nilai tetapan kesetimbangannya perhatikan reaksi berikut. Suatu asam lemah mempunyai harga tetapan ionisasi sebesar. Rumus tetapan hidrolisis garam yang berasal dari asam kuat dan basa kuat.
Sehingga dalam pelarutan asam lemah terjadi kesetimbangan reaksi antara ion yang dihasilkan asam dengan molekul asam yang terlarut dalam air. Modal Minimum 7952 miliar rupiah. Yang diketahui adalah.
Tetapan Kesetimbangan Asam Basa. α akar Kb C. Rumus Menghitung Kebutuhan Kecupkupan Modal Minimum Bank.
CH 3 COONa NaF Na 2 CO 3 KCN CaS. Modal Minimum ATMR x 8. Garam dari asam lemah dan basa lemah.
Tetapan Ionisasi Ka 1 x 10-5 Maka untuk mencari derajat ionisasinya kita gunakan rumus. 4 - log 5 D. 3 - log 2 C.
Untuk menghitung pH asam lemah dan basa lemah diperlukan tetapan kesetimbangan Ka atau Kb terutama sekali. Kecukupan penyediaan modal minimum KPMM atau Modal minimum yang harus dimiliki oleh bank dapat dihitung dengan menggunakan persamaan berikut. CH3COO-aq Haq CH3COOHaq Rumus pH Larutan Buffer Asam.
Garam dari Asam Lemah dan Basa. Pangkat Konsentrasi ion OH- dari hidroksilamin bisa kita dapatkan dari PH nya dengan cara. HCl g NH3 g NH4Cl s HCl Asam.
M 10-5. Garam dari Asam Kuat dan Basa Kuat. OH- Kb x bvalxg atau pOH p Kb - log bg pH 14 - pOH Ket.
M A s M aq A aq x y y x x y Sesuai dengan kaidah penulisan rumus tetapan kesetimbangan hanya zat-zat dalam bentuk larutan aq dan gas g yang dituliskan dalam rumus tersebut. NaCl K 2 SO 4 BaNO 3 2. Kb tetapan ionisasi basa lemah b konsentrasi basa lemah.
Di bawah ini adalah rumusnya. Modal Minimum 994 x 8. Tetapan ionisasi Ka M asam lemah 002 M M Rumus untuk mementukan konsentrasi H dari asam lemah.
Kb tetapakn disosiasi basa. 2 - log 3 B. Molaritas total adalah pencampuran berbagai zat kimia dalam satu wadah yang ditentukan molaritas keseluruhannya berdasarkan rumus.
Reaksi ionisasi basa lemah juga merupakan reaksi kesetimbangan dimana tetapan kesetimbangan untuk reaksi ini adalah tetapan ionisasi basa Kb yang juga disebut tetapan disosiasi basa dengan rumus. Karena perbandingan H dan OH sama maka larutan bersifat netral sehingga kita tidak memerlukan Kh untuk menghitung pH larutan tersebut karena sudah dipastikan pH 7. Jika konsentrasi asam tersebut adalah 002 M maka pH larutan asam tersebut adalah.
 Ph Larutan Dan Reaksi Ionisasi Air
Ph Larutan Dan Reaksi Ionisasi Air
 Contoh Soal Struktur Atom Dan Kunci Jawabannya Pilihan Ganda Struktur Atom Adalah Teori Terhadap Nukleus Di Pusat Atom Kimia Atom Hidrogen Rumus Struktur
Contoh Soal Struktur Atom Dan Kunci Jawabannya Pilihan Ganda Struktur Atom Adalah Teori Terhadap Nukleus Di Pusat Atom Kimia Atom Hidrogen Rumus Struktur
 Waspada Menentukan H Dan Oh Dalam Larutan Garam Terhidrolisis Urip Dot Info
Waspada Menentukan H Dan Oh Dalam Larutan Garam Terhidrolisis Urip Dot Info
 Apa Rumus Ph Larutan Asam Kuat Larutan Asam Lemah Larutan Basa Kuat Larutan Basa Lemah Brainly Co Id
Apa Rumus Ph Larutan Asam Kuat Larutan Asam Lemah Larutan Basa Kuat Larutan Basa Lemah Brainly Co Id
 Pengertian Larutan Penyangga Dapar Serta Sifat Dan Rumusnya
Pengertian Larutan Penyangga Dapar Serta Sifat Dan Rumusnya
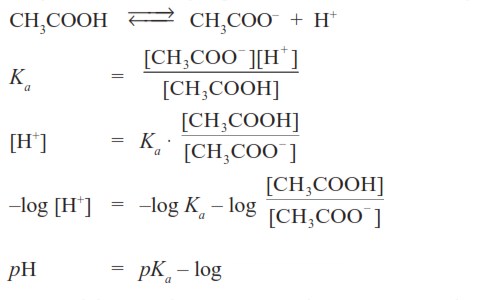 Rumus Untuk Menghitung Ph Larutan Penyangga Rumus Kimia
Rumus Untuk Menghitung Ph Larutan Penyangga Rumus Kimia
 Larutan Asam Basa Kekuatan Derajat Keasaman Contoh Soal
Larutan Asam Basa Kekuatan Derajat Keasaman Contoh Soal
 Cara Menghitung Ph Asam Lemah Dan Basa Lemah
Cara Menghitung Ph Asam Lemah Dan Basa Lemah
 Benzena Dan Turunannya Tata Nama Sifat Sintesis Dan Kegunaannya Benzena Adalah Senyawa Hidrokarbon Aromatik Dengan Rumus Rumus Kimia Kimia Atom Hidrogen
Benzena Dan Turunannya Tata Nama Sifat Sintesis Dan Kegunaannya Benzena Adalah Senyawa Hidrokarbon Aromatik Dengan Rumus Rumus Kimia Kimia Atom Hidrogen
 Cara Mencari Ka Kb Dan Derajat Ionisasi Dari Asam Dan Basa Lemah Panduan Kimia Riset
Cara Mencari Ka Kb Dan Derajat Ionisasi Dari Asam Dan Basa Lemah Panduan Kimia Riset
 Teori Asam Basa Susilawatiamdayani
Teori Asam Basa Susilawatiamdayani
 Rumus Termodinamika Entropi Contoh Soal Dan Jawaban Lubang Hitam Matematika Fisika
Rumus Termodinamika Entropi Contoh Soal Dan Jawaban Lubang Hitam Matematika Fisika
 Senyawa Turunan Alkana Gugus Fungsi Tata Nama Dan Keisomeran Kimia Rumus Kimia Atom Hidrogen
Senyawa Turunan Alkana Gugus Fungsi Tata Nama Dan Keisomeran Kimia Rumus Kimia Atom Hidrogen
 Contoh Soal Benzena Dan Turunannya Pilihan Ganda Beserta Jawabannya Benzena Adalah Senyawa Hidrokarbon Aromatik Dengan Rumus Kimia Rumus Kimia Rumus Struktur
Contoh Soal Benzena Dan Turunannya Pilihan Ganda Beserta Jawabannya Benzena Adalah Senyawa Hidrokarbon Aromatik Dengan Rumus Kimia Rumus Kimia Rumus Struktur
 Cara Menghitung Ph Larutan Penyangga Asam Dan Basa
Cara Menghitung Ph Larutan Penyangga Asam Dan Basa
 How To Take My Notes Chemistry Perasaan
How To Take My Notes Chemistry Perasaan
 Termokimia Rumus Penjelasan Beserta Contoh Soal Dan Jawaban Fisika Kimia Matematika
Termokimia Rumus Penjelasan Beserta Contoh Soal Dan Jawaban Fisika Kimia Matematika
 Cara Menghitung Ph Asam Lemah Dan Basa Lemah
Cara Menghitung Ph Asam Lemah Dan Basa Lemah
 Rumus Massa Garam Dalam Materi Asam Basa Brainly Co Id
Rumus Massa Garam Dalam Materi Asam Basa Brainly Co Id