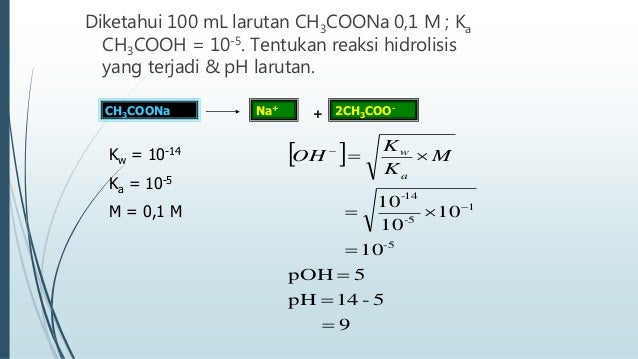
Volume larutan sebanyak 250 mL 025 L. Sebanyak 100 mL larutan CH3COOH 02 M dicampur dengan 100 mL larutan NaOH 02 M.
 Nilai Ph Larutan Garam Nh4cl 0 1 M Yang Memiliki Tetapan Hidrolisis Kh 10 9 Adalah Brainly Co Id
Nilai Ph Larutan Garam Nh4cl 0 1 M Yang Memiliki Tetapan Hidrolisis Kh 10 9 Adalah Brainly Co Id
Terdapat 10 L larutan NH42SO4 01 M.

Tetapan hidrolisis garam nh4cl 0 1 m adalah. 50 mL CH 3 COOH 02 M dan 100 mL NH4OH 01 M. 100 ml HCl 01 M 100 ml NaOH 01 M d. Konsentrasi garam NaCN yang diperlukan sebesar 10-4 M.
Diketahui Ka CH3COOH 175 x 10-5 molL dan Kb NH3 18 x 10-5 molL berapakah nilai tetapan hidrolisis adalah. 513 x 10 -5 molL b. 1Jika 50 mL larutan KOH 05 M dicampurkan dengan 50 mL larutan CH3COOH 05 M maka hitung pH campuran yang terjadi Ka 10-6.
Tetapan hidrolisis garam nh4cl 01 m adalah kb nh3 10-5 - 14782235 13. Kb 10 5. Mol Volume x Molar Mol 025 x 10 -4 25 x 10 -5 mol.
Hidrolisis garam adalah penguraian garam oleh air atau reaksi ion-ion garam oleh air. Konsentrasi CH3COO- dalam campuran adalah 01 M Pembahasan. Terdapat 10 L larutan garam NH4CH3COO 025 M.
Konsentrasi H dalam larutan tersebut adalah. M NH 4 Cl 01 M. Ke dalam 1 liter larutan asam asetat 02 M ditambahkan padatan NaOH 8 gram.
Kebalikan dari tetapan hidrolisis garam asam kuat dan basa lemah hidrolisis asam lemah dan basa kuat bersifat basa pH 7. NH4 merupakan asam konjugasi kuat dari NH 4 OH maka NH4 yang mengalami hidrolisis. Terdapat 10 L larutan garam NH 4 CH 3 COO 025 M.
Tentukan nilai tetapan hidrolisis Kh NH4Cl 01 M Kb NH4OH 18. Garam-garam yang mengalami hidrolisis adalah garam yang mengandung ion dari asam lemah atau basa lemah. 513 x 10 -5 molL.
Konsentrasi dari NH4Cl 04 M jika kb NH3 10-5. Rumus Menghitung Tetapan Hidrolisis Garam NH 4 Cl. Sedangkan garam yang berasal dari asam kuat atau basa kuat tidak bisa mengalami reaksi hidrolisis.
Jika Ka CH3COOH 1 x 10-5 maka pH larutan setelah dicampur adalah. Derajat ionisasi 10 atau 01. NaX 01 M.
Dengan demikian nilai tetapan hidrolisis garam adalah dan pH larutan garamnya adalah 12. Diketahui K a CH 3 COOH 175 x 10-5 molL dan K b NH 3 18 x 10-5 molL berapakah nilai tetapan hidrolisis adalah. 472 x 10 -5 molL.
Campuran larutan berikut ini yang membentuk larutan penyangga adalah. Jika Kb NH4OH 2x10-5 tentukanlah pH larutan garam tersebut. Sebanyak 107 gram garam NH4Cl Mr 535 dilarutkan dalam air hingga volumenya 100 mL.
100 ml HCl 01 M 100 ml NH4OH 01 M e. 100 ml HF 01 M 100 ml KOH 01 M c. 4 Tetapan Hidrolisis Kh dan pH larutan Garam yang Berasal dari Asam Lemah dan Basa Lemah a Kh larutannya Page 10 Hidrolisis Garam Perhitungan Kh larutan garam yang berasal dari asam lemah dan basa lemah dapat dilakukan seperti cara berikut.
100 ml HCOOH 01 M 100 ml KOH 01 M Chemistry 2B Nana Sutresna Facil 2010 h. Jika tetapan hidrolisis Kh 1 x 10-9 maka pH larutan garam adalah. Rumus tetapan hidrolisis garam yang berasal dari asam lemah dan basa kuat.
Konsentrasi kation dari garam. Seorang siswa mempelajari reaksipengendapan dengan mencampurkanberbagai larutan berikutPercobaan2Campuran larutan10 mL Caso 01 M dan10 ml Na. M 2.
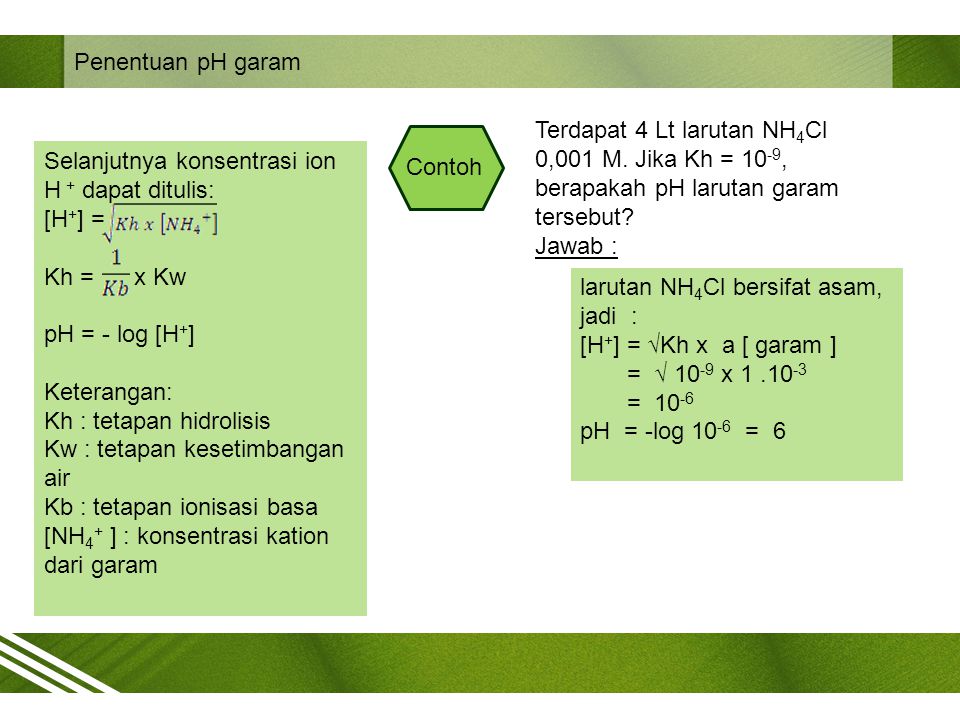
BH aq H 2 O l B aq H 3 O aq. 50 mL CH 3 COOH 02 M dan 50 mL NH 4 OH 01 M. ContohTerdapat 4 Lt larutan NH4Cl 0001 M.
Maka rumus tetapan hidrolisis garamnya adalah sebagai berikut. Jadi CH3COONa yang diperlukan sebanyak 094 gram. Larutan NH4Cl 04 M memiliki tetapan hidrolisis sebesar 109.
Kh B x H 3 O. Jika 107 mg garam NH4Cl dilarutkan dalam air hingga 1 L konstanta hidrolisis 10-9 tentukanlah pH larutan garam tersebut. Dengan demikian mol garam NaCN yang dibutuhkan adalah.
Ion ion yang dihasilkan dari ionisasi garam yang berasal dari asam. Larutan garam NH4Cl 01 M mengalami hidrolisa menurut reaksi. 152 Jawaban.
Jika Kb NH4OH 2 x 10-5 pH larutan garam yang tersebut sebesar. Tetapan hidrolisis Kw. Konsentrasi Na dalam campuran adalah 005 M E.
NH 4 Cl akan terionisasi sempurna dalam air dan membentuk NH4 dan Cl. Tetapan ionisasi basa NH4. 50 mL CH 3 COOH 02 M dan 100 mL NaOH 01 M.
Jika Kh 10-9 berapakah pH larutan garam tersebutJawab larutan NH4Cl bersifat asam jadi H Kh x a garam 10-9 x 1 10-3 10-6pH -log 10-6 6. 50 mL CH 3 COOH 02 M dan 50 mL NaOH 01 M. Tetapan kesetimbangan air Kb.
NH4Cl NH4 Cl. Berikut adalah tahapan dalam menentukan Kh garam dan pH larutan garam. HIDROLISIS GARAM Adalah pengertian definisi materi makalah rumus macam-macam dan contoh soal hidrolisis garam beserta pembahasannya.
50 mL CH 3 COOH 02 M dan 50 mL NaOH 01 M. 2 104 D. 100 ml CH3COOH 01 M 100 ml NaOH b.
Hitung tetapan hidrolisis dan pH larutan garam NH 4 Cl 01 M jika harga Kb 10 5.
 Diketahui Kb Nh3 1 8 X 10 6 Tentukan A Ph Larutan Nh4cl 0 2 M B Tetapan Hidrolisis Kh Brainly Co Id
Diketahui Kb Nh3 1 8 X 10 6 Tentukan A Ph Larutan Nh4cl 0 2 M B Tetapan Hidrolisis Kh Brainly Co Id
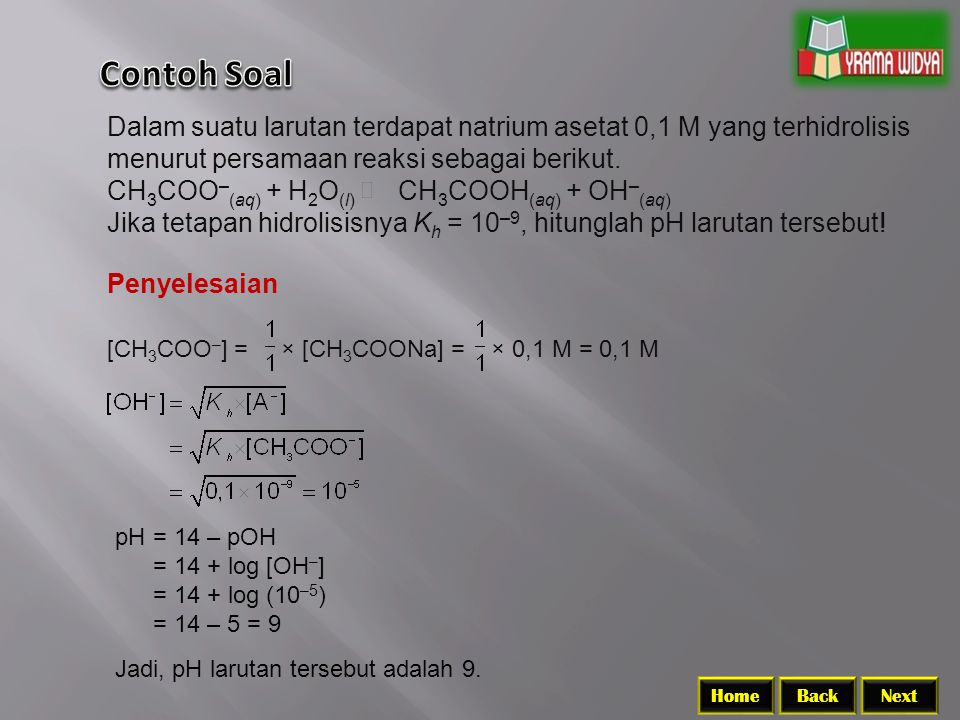 Bab 7 Larutan Penyangga Dan Hidrolisis Next Ppt Download
Bab 7 Larutan Penyangga Dan Hidrolisis Next Ppt Download
 Rangkuman Materi Contoh Soal Hidrolisis Pembahasan Kelas 11
Rangkuman Materi Contoh Soal Hidrolisis Pembahasan Kelas 11
 Hidrolisis Garam Dan Buffer Ppt Download
Hidrolisis Garam Dan Buffer Ppt Download
 Soal Dan Pembahasan Hidrolisis Garam Kimia
Soal Dan Pembahasan Hidrolisis Garam Kimia
 50 Ml Larutan Nh4cl 0 05 M Jika Tetapan Hidrolisis Kh Garam 10 8 Maka Tentukan Ph Larutan Brainly Co Id
50 Ml Larutan Nh4cl 0 05 M Jika Tetapan Hidrolisis Kh Garam 10 8 Maka Tentukan Ph Larutan Brainly Co Id
 Soal Dan Pembahasan Hidrolisis Garam Kimia
Soal Dan Pembahasan Hidrolisis Garam Kimia
 Soal Dan Pembahasan Hidrolisis Garam Kimia
Soal Dan Pembahasan Hidrolisis Garam Kimia
 Hidrolisis Garam Rudi Purwanto Ppt Download
Hidrolisis Garam Rudi Purwanto Ppt Download
 Hidrolisis Garam1 Perkirakan Ph Larutan Berikut A Nh4cn B Nh4f Diketahui Ka Hcn 6 2 X Brainly Co Id
Hidrolisis Garam1 Perkirakan Ph Larutan Berikut A Nh4cn B Nh4f Diketahui Ka Hcn 6 2 X Brainly Co Id
 Larutan Nh4cl 0 4m Memiliki Hidrolis Sebesar 10 Pangkat 9 Tentukan Ph Hidrolis Tersebut Brainly Co Id
Larutan Nh4cl 0 4m Memiliki Hidrolis Sebesar 10 Pangkat 9 Tentukan Ph Hidrolis Tersebut Brainly Co Id
 Tetapan Hidrolisis Suatu Garam Yang Diperoleh Dari Asam Lemah Dan Basa Kuat Adalah 1 0 X10 10 Brainly Co Id
Tetapan Hidrolisis Suatu Garam Yang Diperoleh Dari Asam Lemah Dan Basa Kuat Adalah 1 0 X10 10 Brainly Co Id
 Larutah Nh4cl 0 1 M Terhidrolisis 1 Berapa Tetapan Hidrolisis Dan Ph Larutan Brainly Co Id
Larutah Nh4cl 0 1 M Terhidrolisis 1 Berapa Tetapan Hidrolisis Dan Ph Larutan Brainly Co Id
 Kerjakan Soal Berikut 1 Diketahui Larutan 0 1 M Nh4cl Dan Kb Nh4oh 10 5 A Tuliskan Hidrolisis Brainly Co Id
Kerjakan Soal Berikut 1 Diketahui Larutan 0 1 M Nh4cl Dan Kb Nh4oh 10 5 A Tuliskan Hidrolisis Brainly Co Id
 Hidrolisis Garam Erma Nurhidayati Ppt Download
Hidrolisis Garam Erma Nurhidayati Ppt Download
 Hitunglah Ph Larutan Nh4cl 0 1 M Kb Nh4oh 1 10 5 Brainly Co Id
Hitunglah Ph Larutan Nh4cl 0 1 M Kb Nh4oh 1 10 5 Brainly Co Id
 Larutan Garam Nh4c10 1m Mengalami Hidrolisis Menurut Reaksi Brainly Co Id
Larutan Garam Nh4c10 1m Mengalami Hidrolisis Menurut Reaksi Brainly Co Id