Lambang L menyatakan huruf pertama dari Loschmidt seorang ilmuwan austria yang pada tahun 1865 dapat menentukan besarnya tetapan Avogadro dengan tepat. Maka 2 1 2 1 n n V V P T 3.
 Hukum Dasar Kimia Dan Perhitungan Kimia
Hukum Dasar Kimia Dan Perhitungan Kimia
Nilai ini kebetulan sangat dekat hanya berbeda 037 lebih kecil dengan 2 79 mol 1 sehingga angka ini berguna sebagai perkiraan pada fisika nuklir pada waktu menghitung laju pertumbuhan reaksi berantai.

Tetapan avogadro sama dengan. Nilai 6022 x 10 23 partikel per mol disebut sebagai tetapan Avogadro dengan lambang L atau N. Jika nilai n dari persamaan reaksi tersebut sama dengan 602 10 23 atau sebesar tetapan Avogadro maka n molekul sama dengan satu mol. Avogadro maka n molekul sama dengan satu mol.
Jika nilai n dari persamaan reaksi tersebut sama dengan 602 1023 atau sebesar tetapan. Bilangan Avogadro lambang. Mr N 1 gram.
Jadi pada suhu dan t ekanan yang sama perbandingan mol gas sama dengan perbandingan volume gas. Tetapi sebenarnya yang Anda reaksikan bukan satu atom karbon dengan satu molekul oksigen melainkan sejumlah besar atom karbon dan sejumlah besar molekul oksigen. Tetapan Avogadro L 6021023 partikelmol.
Konsep Mol dan Tetapan Avogadro - Apabila Anda mereaksikan satu atom karbon C dengan satu molekul oksigen O2 maka akan terbentuk satu molekul CO2. L atau NA juga disebut sebagai ketetapan Avogadro ataupun konstanta Avogadro ialah banyaknya entitas biasanya atom ataupun molekul di dalam satu mol yang juga merupakan jumlah atom karbon-12 dalam 12 gram 0012 kilogram karbon-12 dalam keadaan dasarnya. Tentukan jumlah mol n dalam 1 gram Nitrogen.
2H2O O2 2H2O Tetapan Avogadro L 6021023 partikelmol. Dengan demikian persamaan reaksi tersebut menyatakan perbandingan mol. Hubungan Mol dengan Tetapan Avogadro Kuantitas atom molekul dan ion dalam suatu zat dinyatakan dalam satuan mol.
3 Molaritas Larut an merupakan campuran ant ara pelarut dan zat t erlarut. Sehingga 1 mol emas 6021023 atom emas. Konsep mol didukung oleh adanya bilangan Avogadro yang ditemukan oleh fisikawan italia bernama Amadeo Avogadro.
Dalam kehidupan sehari-hari mol dapat dianalogikan sebagai lusin. Berdasarkan kesepakatan untuk partikel yang jumlahnya sebesar tetapan Avogadro atau 602 10 23 dinyatakan sebesar satu mol. Konsep Mol dan Tetapan Avogadro.
Jika nilai n dari persamaan reaksi tersebut sama dengan 602 10 23 atau sebesar tetapan Avogadro maka n molekul sama dengan satu mol. Dengan demikian persamaan reaksi tersebut menyatakan perbandingan mol. Jadi dalam satu mol suatu zat terdapat 6022 x 10 23 partikel.
Konsep Mol dan Tetapan Avogadro. N massa N. Contohnya adalah 1 mol air mengandung 602214076x1023 partikel air.
Jadi dalam satu mol suatu zat terdapat 6022 x 10 23 partikel. Dengan demikian persamaan reaksi tersebut menyatakan perbandingan mol. Nilai 6022 x 10 23 partikel per mol disebut sebagai tetapan Avogadro dengan lambang L atau N.
Satuan ini dinamakan mol. Sebenarnya tetapan Avogadrolah yang didefinisikan menurut satuan mol tersebut from MATH 101 at Tanjungpura University. Dengan kata lain satu mol setiap zat mengandung 602 10 23 partikel zat baik atom molekul maupun ion.
Jumlah partikel mol n x 602 x 10 23 atau Jumlah partikel n x Tetapan Avogadro. Kata partikel pada NaCl H 2 O dan N 2 dapat dinyatakan dengan. 14 071 mol.
Jika lusin menyatakan jumlah 12 buah mol menyatakan jumlah 6022 x 10 23 partikel zat. Misalnya untuk mendapatkan 18 gram air maka 2 gram gas hidrogen direaksikan dengan 16 gram gas oksigen. Pengertian dan Contoh Soal Fraksi Mol.
L atau N A juga dinamakan sebagai tetapan Avogadro atau konstanta Avogadro. 1 Hubungan mol dengan tetapan Avogadro. Perkiraan terbaik terakhir untuk angka ini adalah.
Kata partikel pada NaCl H 2 O dan N 2 dapat dinyatakan dengan. Jumlah zat t erlarut dalam larut an dinyat akan dalam konsent rasi. Jika lusin menyatakan jumlah 12 buah mol menyatakan jumlah 6022 x 10 23 partikel zat.
Dalam kehidupan sehari-hari mol dapat dianalogikan sebagai lusin. X n x L 0071 x 602x1023 427x1022. Dalam satu mol besi terkandung 602 10 23 atom Fe.
Bilangan Avogadro menyatakan bahwa dalam satu mol zat terdapat partikel sejumlah 602214076x1023. Hubungan mol dengan tetapan Avogadro dapat dinyatakan dengan persamaan rumus berikut. Tentukan banyak partikel X Natrium dalam 071 mol konsentrasinya.
Perkiraan terbaik terakhir untuk angka ini adalah. 2 mol C 1 mol O2 2 mol CO Dapat disimpulkan bahwa koefisien reaksi pada persamaan kimia menunjukkan. Jika tetapan Avogadro L banyaknya atom Nitrogen yang terkandung dalam 1 gram gas Nitrogen adalah Jawaban.
1 mol air 6021023 atom air. 1 mol gula 6021023 molekul gula.
 Apa Itu Bilangan Avogadro Dan Rumus Avogadro Brainly Co Id
Apa Itu Bilangan Avogadro Dan Rumus Avogadro Brainly Co Id
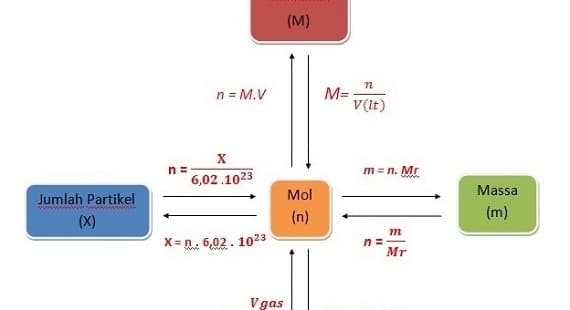 Pengertian Konsep Rumus Mol Radenwinata Com
Pengertian Konsep Rumus Mol Radenwinata Com
 Konsep Mol Dan Stoikiometri Beranda Ki Kd Kimia
Konsep Mol Dan Stoikiometri Beranda Ki Kd Kimia
 Catatan Sekolahku Kimia Konsep Mol
Catatan Sekolahku Kimia Konsep Mol
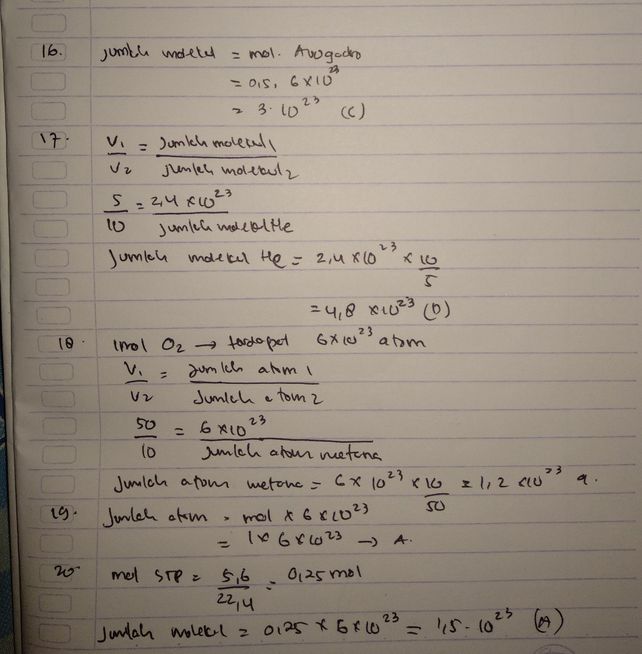 Pada Suhu Dan Tekanan Ya Descubre Como Resolverlo En Qanda
Pada Suhu Dan Tekanan Ya Descubre Como Resolverlo En Qanda

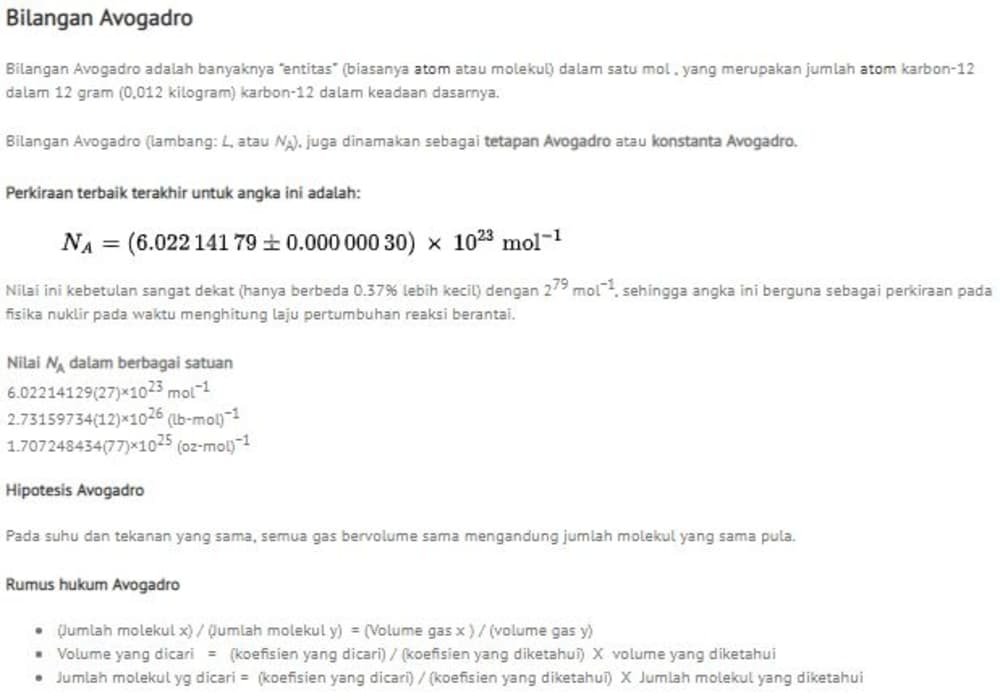 Avogadro Bilangan Hipotesis Avogadro Reaksi Kimia Soal Jawaban
Avogadro Bilangan Hipotesis Avogadro Reaksi Kimia Soal Jawaban
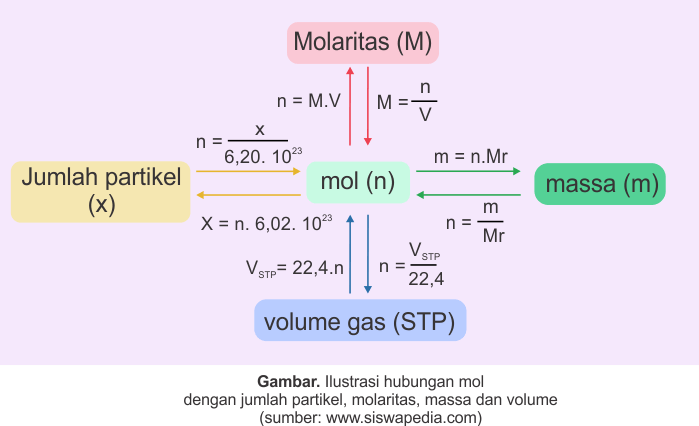 Pengertian Dan Rumus Satuan Mol Siswapedia
Pengertian Dan Rumus Satuan Mol Siswapedia
 Jumlah Partikel Yang Terkandung Dalam Setiap Satu Mol Zat Adalah Brainly Co Id
Jumlah Partikel Yang Terkandung Dalam Setiap Satu Mol Zat Adalah Brainly Co Id
 Konsep Mol Dan Tetapan Avogadro
Konsep Mol Dan Tetapan Avogadro
 Contoh Soal Mol Dan Penyelesaiannya Pembahasan Soalfismat Com
Contoh Soal Mol Dan Penyelesaiannya Pembahasan Soalfismat Com







